《集采的仿制药,其质量真的可以通过一致性评价吗?》
很多医学界同仁根据自身的临床所见,质疑集采药物质量不可靠。
然而,他们提出质疑的理由居然是“我见到的某个案例”,“我的经验”,我感觉到的……
根据某个案例,根据个人经验,就痛批通过“疗效一致性评价”的药物,这完全不是医学专业人士该有的专业素养。
医生当然可以反馈药物质量问题,对个案的反馈,可以通过药物副反应反馈体系;如果认为有超一般的药物副反应问题,怀疑这类药物的质量有问题,那就应该拿出可信的研究数据来说话。
但是,我们的医生没能体现出该有的专业素养,反而是说个案,说个人经验,这非常让人失望。
不过,不是所有人都这样。
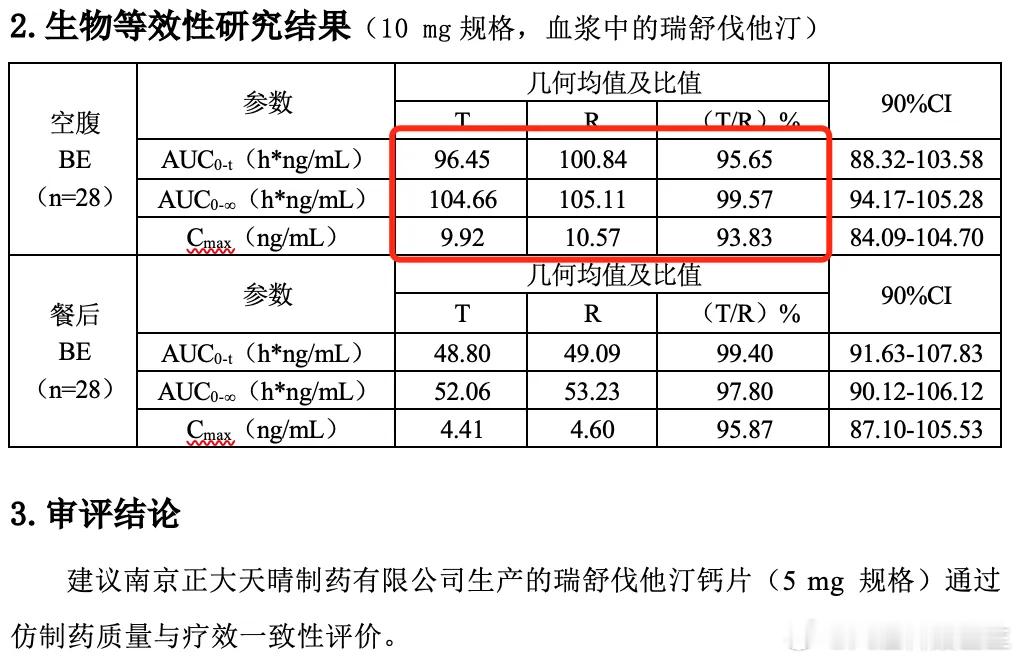
我曾经的领导,专业素养过硬的夏志敏医生就发文指出:根据公开披露的信息来看,某些仿制药的生物等效性研究的数据居然惊人的完全一样。
他的原文如下(具体见他微信公众号里的文章):
……
一个仿制药要正规通过一致性评价,难度很大,要求非常高。我国 6000-7000 家药企,数以万计的仿制药,到目前通过一致性评价的也才 1988 个品规。
除了需要通过实验室的质量标准检测,还需要在人体试验中验证其生物等效性。而这些验证方法和流程,不论美国日本,基本是国际惯例。
……如此严肃认真的生物等效性研究,却出现了大面积的数据雷同。
难怪有人质疑,并不是仿制药质量不好,而是中国仿制药质量太差。
中国仿制药,劣币继续驱除良币据仿制药领域资深人士透露,上述情况并不意外。一致性评价早期,有的公司实打实做,三次才通过,生物等效性验证成本 3000 万以上,而后来同品种其他公司 800 万包过。
据猜测,这样的数据雷同,不排除第三方公司分包给了同一家下游公司,导致数据完全一致。否则同一品种的竞争对手公司怎么可能轻易地共享数据?
始于 2012 年的一致性评价,本来很有希望扭转中国制药劣币驱除良币的糟糕状况。但在 2018 年集采即将启动之前,一致性评价开始加速,各省药监在验产等环节也开始放水。
10轮集采,始终坚持低价中标,外资原研已经全部离场,一些实实在在做的仿制药企,成本高,即使中标也位于尾部,得到的采购量很少,生存越来越难。
=========
这是一个非常严肃的,有可信证据的指控。即,我们的仿制药的药效一致性评价,真的可靠吗?
当公开披露的信息如此雷同的情况下,我们对药效一致性评价的真实性,可靠性是必然要怀疑的。
、、
还是那句话,我并不是反对质疑“集采药的质量”,而是我们的质疑应该有可信的证据、合理的逻辑。
如果我们的质疑是基于个案,基于所谓的个人经验,作为普通人还可以接受,作为医生那就太不把自己的招牌当回事了。
而夏志敏老师的质疑才能算对得起医生这个称号。
评论列表