转自:医学界
HER2阳性乳腺癌治疗变革中,肿瘤浸润细胞(TILs)是影响新辅助治疗反应的关键因素。
乳腺癌是全球女性中最常见的恶性肿瘤之一,其不同分子亚型的生物学特征及临床转归呈现出显著差异。其中,HER2阳性乳腺癌因具有显著的侵袭性表型和不良预后特征,始终是乳腺癌研究领域的重要方向。近年来,TILs因其在肿瘤免疫应答中的重要作用而在肿瘤学领域受到广泛关注,多项研究证实TILs在HER2阳性乳腺癌新辅助治疗中具有重要价值。研究表示,高TILs的水平已被证明与治疗反应和生存结果相关,尤其是在三阴性乳腺癌和HER2阳性乳腺癌中[1,2]。2025年4月,《Oncologist》在线发表了一篇名为“Tumor-infiltratinglymphocytesaspredictivebiomarkersinneoadjuvanttreatmentofHER2-positivebreastcancer”的文章[3],探讨了TILs在HER2阳性乳腺癌新辅助治疗中的作用,为优化治疗策略提供了新的视角。本文精粹研究相关内容,以飨读者。
研究设计
本研究为一项回顾性单中心分析,研究者回顾了435名接受新辅助治疗的乳腺癌患者,根据TIL水平对患者进行分层,过程如图1所示。这些患者均接受了由蒽环类药物、紫衫烷、曲妥珠单抗和帕妥珠单抗组成的新辅助治疗方案,每三周静脉注射一次。研究主要终点为病理完全缓解率(pCR),次要终点为无病生存期(DFS),定义为从首次开始新辅助治疗到复发或最后一次对照日期的时间。
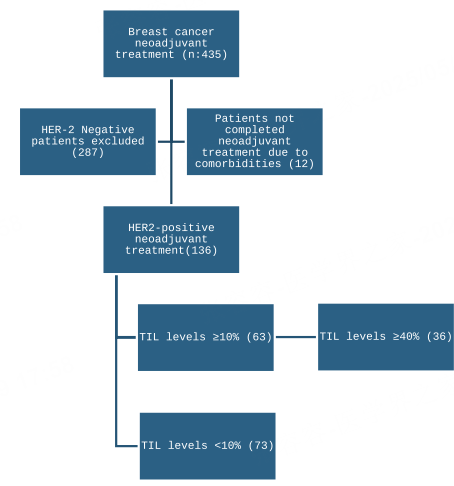
1.接受新辅助治疗的乳腺癌患者的选择过程
TILs的评估主要基于使用苏木精和伊红染色的肿瘤组织切片进行,评估遵循国际TILs工作组的建议。TIL水平被分为低(TILs:0%-10%)、中(TILs:10%-40%)和高(TILs:>40%)。所有TIL评估过程由一位不知情患者结果的病理学家进行。此外,研究还考虑了其他临床和病理变量,如Ki67水平、肿瘤大小和淋巴结状态等。
研究结果
1患者特征
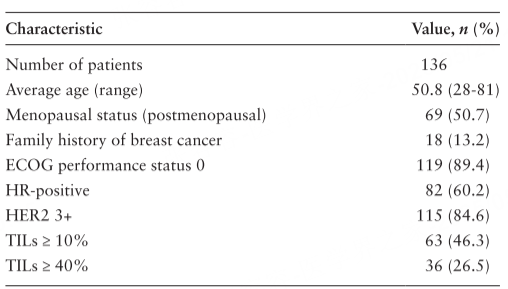
研究纳入了136例诊断为HER2阳性乳腺癌的患者,人群特征如表1所示。这些患者的平均年龄是50.8岁,均为女性。其中,60.2%的患者HR阳性,46.3%的患者为中TIL水平,26.5%的患者为高TIL水平。
表1.患者特征和人口统计学
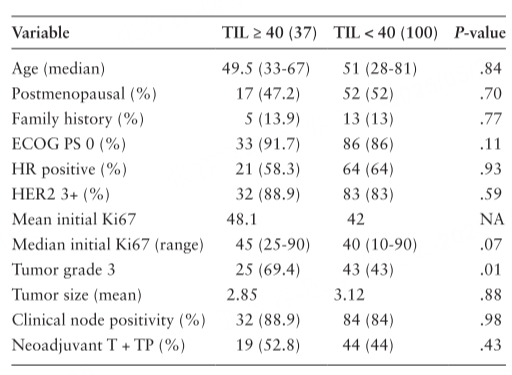
同时,研究者还比较了基线高水平和低水平TILs组的各种临床和病理变量(图3)。TIL≥40%组和TIL<40%组的中位随访时间为33.6个月。TIL临界值为40%时,除肿瘤分级外,大多数参数无统计学意义差异,肿瘤分级在TIL≥40%组中显著升高(P=0.01)。
表2.基线TIL≥40组和TIL<40组的变量比较
2pCR率与TIL水平的相关性
研究发现,高TIL水平与更高的pCR率显著相关(60.32%vs.39.73%,p=0.02),特别是TIL水平高于40%阈值的情况下,这表明TIL水平是预测pCR的重要指标(图2)。
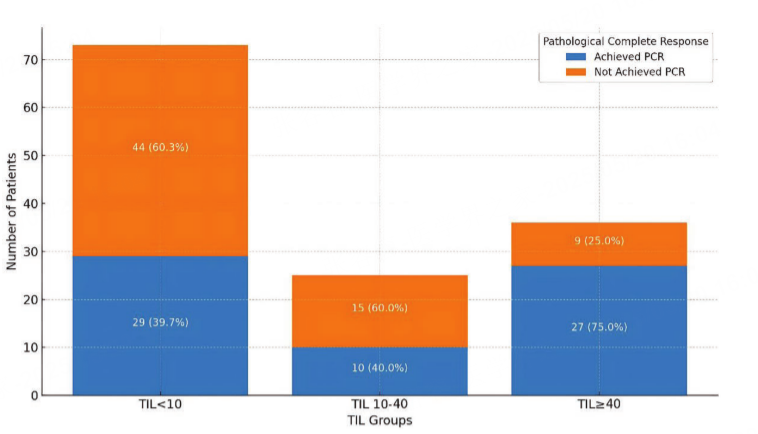
2.TIL组的病理完全缓解率
logistic分析进一步发现,淋巴结受累(P=0.004,OR=1.805)和TIL≥40%(P=0.010,OR=4.998)是pCR的重要预测因素。TIL≥10%在单因素分析中显示出与pCR相关,但在回归模型中没有统计学意义(P=0.470,OR=1.453)。这些结果证明了TIL≥40%作为治疗反应可靠预测指标的潜力,且较高的TIL水平对于识别可能从新辅助治疗中受益的患者有特别价值。
3DFS与TIL水平的相关性
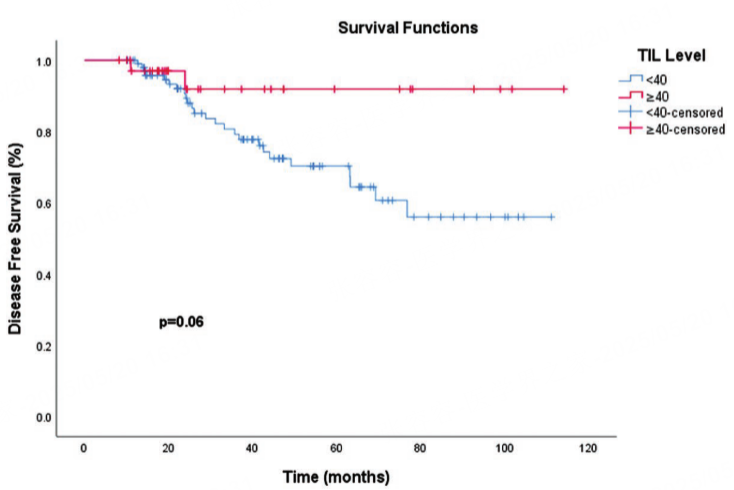
在DFS分析中,TIL水平未显示出显著预后价值:TIL<10%组(平均DFS为84.3个月,95%Cl,72.9个月-95.7个月)与TIL≥10%组(平均DFS为89.0个月,95%Cl,77.3个月-100.8个月)差异无统计学意义(P=0.868)(图3)。但值得注意的是,TIL≥40%患者的平均DFS为106.4个月(95%Cl,95.9个月-116.9个月),显著高于TIL<40%组的80.9个月(95%Cl,71.4个月-90.5个月)(P=0.062)。尽管未达统计学显著性,但也表明TIL≥40%的患者有潜在的DFS获益趋势。此外,高TIL组的DFS趋势有所改善,3年高TIL组生存率为91.9%,低TIL组为80.7%,这一趋势仍提示TIL水平对长期生存可能具有积极影响。
3.TIL和Ki67组的病理缓解率(pCR)
4Ki67水平与TIL水平对治疗反应的影响
在TIL水平较低的患者中,高Ki67表达与更好的pCR率相关(57.10%vs.30.80%,P=0.010)(图4)。而在高TIL患者中,高Ki67和低Ki67组之间没有显著差异(P=0.317)。这一结果提示,TIL丰度可能动态调节Ki67表达与治疗反应的相关性,在TIL富集的微环境中,Ki67抑制剂可能具有更稳定的疗效响应特征。
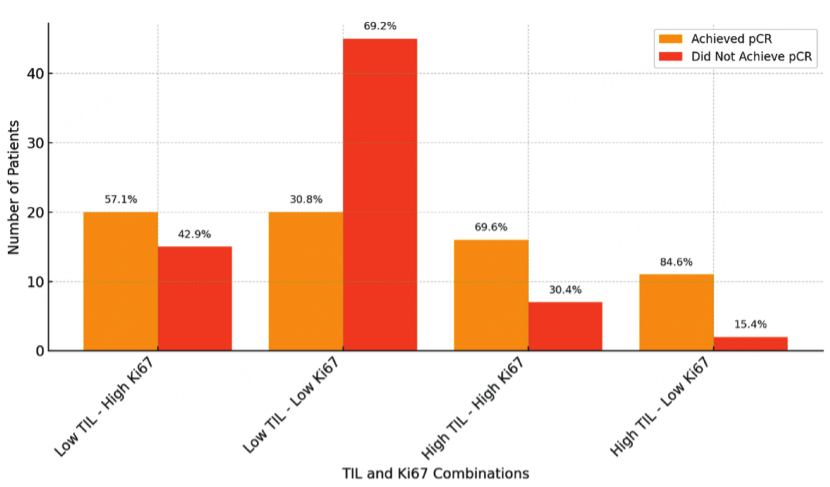
4.TIL和Ki67组的病理缓解率(pCR)
5安全性
尽管该研究未详细报告不良反应的具体数据,但其他相关研究显示,在HER2阳性乳腺癌的新辅助治疗中,使用蒽环类和抗HER2治疗的不良反应主要集中在心脏毒性、骨髓抑制和胃肠道反应等方面[4]。例如,蒽环类药物的心脏毒性可能导致心功能下降,表现为左心室射血分数(LVEF)降低。通过合理调整剂量和监测,这些不良反应通常可以得到有效管理。此外,抗HER2治疗(如曲妥珠单抗)也可能引发心肌病等心脏不良事件,但发生率相对较低。在本研究中,未报告与TIL水平相关的特殊不良反应。
研究总结
本研究强调了TILs在HER2阳性乳腺癌新辅助治疗中的预测潜力。TIL水平与pCR和DFS显著相关,提示其可作为预后和治疗反应的生物标志物。在临床实践中,TILs的评估有助于制定个性化治疗方案,优化治疗效果。未来需进一步验证TILs的作用机制,标准化评估方法,进一步探索其在乳腺癌精准诊疗中的应用潜力。
参考文献:
[1].SalgadoR,DenkertC,CampbellC,etal.Tumor-infiltratinglym-phocytesandassociationswithpathologicalcompleteresponseandevent-freesurvivalinHER2-positiveearly-stagebreastcancertreatedwithlapatinibandtrastuzumab:asecondaryanalysisoftheNeoALTTOtrial.JAMAOncol.2015;1:448-454.
[2].韩佳雯,苏婷婷,徐元兵,等.肿瘤浸润淋巴细胞在三阴性乳腺癌新辅助化疗预测价值中的研究进展[J].中国肿瘤临床,2023,50(19):1011-1016.
[3].KınıkoğluO,AltıntaşYE,YıldızA,etal.Tumor-infiltratinglymphocytesaspredictivebiomarkersinneoadjuvanttreatmentofHER2-positivebreastcancer.Oncologist.2025;30(4):oyaf054.
[4].Cathcart-RakeEJ,TevaarwerkAJ,HaddadTC,etal.Advancesinthecareofbreastcancersurvivors.BMJ.2023Sep18;382:e071565.
本材料由阿斯利康提供,仅供医疗卫生专业人士参考
审批编号:CN-163299,有效期2026-07-08