封面新闻记者谭羽清
据世界卫生组织(WHO)数据,全球每年只有不到10%的器官移植需求能得到满足。而随着基因编辑技术和免疫学的飞速发展,异种器官移植研究有望成为解决全球器官短缺难题的有效方式。
近日,我国在异种移植领域再次取得重大突破。3月6日,在中国科学院窦科峰院士指导下,西京医院医疗团队将一颗6基因编辑猪的肾脏成功移植至一位终末期肾病患者体内。截至3月12日,这颗“猪肾脏”在患者体内状态良好,血肌酐已恢复正常水平。
据悉,此次“多基因编辑猪-终末期肾病患者”异种肾移植手术由中国科学家独立自主实施,为亚洲首例、全球第五例。提供肾脏的基因编辑猪则是由中国科技企业成都中科奥格自主研发、培育而成。
“本次手术的成功,是我国异种移植在活体病人的一个开端。”3月13日,中科奥格创始人、董事长潘登科博士在接受封面新闻记者采访时表示,本次手术对我国异种器官移植研究走向临床试验有着助推作用。
终末期肾病患者成功移植“猪肾脏”
西京医院资料显示,本次接受基因编辑猪肾脏异种器官移植手术的是一位69岁的终末期肾病患者。其患有严重的高血压、糖尿病等基础疾病,药物服用史已有30多年。
8年前,这位患者又被诊断为慢性肾功能不全尿毒症期,换肾、透析成了其延续生命的唯二选择。而考虑到合并症较多,且为肾移植高致敏患者,没有适合配型要求的肾源,该患者只能通过每周三次的透析维持生命。
但随着时间推移,透析并发症接踵出现,该患者又发生了脑梗、心梗,令身体状况进一步恶化。得知西京医院在开展系列异种肾脏移植研究的消息后,这位患者的家人经深思熟虑,带其前往咨询,并最终决定尝试这一治疗方案。
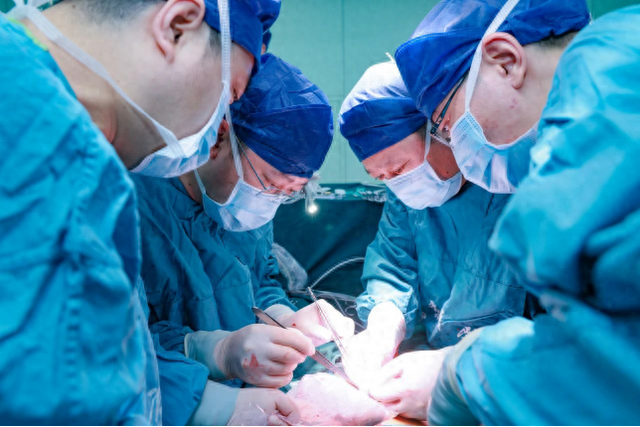
在征得患者和家属充分信任和支持后,团队在结合既往动物实验及脑死亡受体异种肾移植的研究基础上,尝试进行突破性探索,最终顺利完成移植手术。术中,移植肾脏恢复血流后,色泽红润,随即产生尿液。超声显示肾脏血流灌注良好,未发生超急性排斥反应。术后第6天,该位患者生命体征平稳,移植肾功能良好,24小时尿量最高达到5468ml,血肌酐术后第三天已降至正常水平,尿素由术前的23.91mmol/L降至10.01mmol/L……这一系列积极的现象标志着手术已初步取得成功。
西京医院泌尿外科秦卫军主任介绍,目前处于移植后早期阶段,下一步,团队将持续监测患者和移植肾脏的状态指标,并结合前期预案,进一步做好免疫排斥、凝血障碍、病原感染等难关攻克。
据了解,西京医院在异种肾脏移植临床研究方面有着坚实基础。2016年以来,该医院泌尿外科就先后开展及参与了多例“基因编辑猪-猴”异种肾移植和肝肾联合移植研究,并在2024年3月成功实施“多基因编辑猪-脑死亡受体”异种肾移植。
“亚洲首例”的背后是超20年技术积累
培育出符合要求的基因编辑供体猪,是异种器官移植研究得以发展的基础与关键。近日亚洲首例“多基因编辑猪-终末期肾病患者”异种移植手术能成功开展,其背后离不开潘登科团队超20年的技术积累。

中科奥格建在山间的基因编辑猪繁育中心(摄于2023年)
据潘登科介绍,早在2003年,团队就开始了基因编辑猪异种器官移植最底层的技术积累,进行克隆猪研究。2010年,他们培育出中国第一头“抗超急性免疫排斥基因猪”,正式打开中国异种大器官移植新时代。

潘登科团队培育的基因编辑猪
随后,自2013年起,潘登科团队开始持续为全国多个器官移植中心提供移植用猪,并陆续与多家医院展开合作,在不断优化供体猪的同时,推动基因编辑异种器官移植研究一步步从“猪-猴”过渡至“猪-脑死亡受体”。
为了避免供体猪在培育过程中受到外界病原微生物等因素的侵袭,导致猪的疾病通过异种器官移植传染给人,潘登科团队于2022年建成了DPF(DesignatedPathogenFree)医用供体猪培育中心,该设施能为其中的供体猪提供相当于医院手术室级别的超洁净级环境。

截至目前,潘登科团队已完成超60例“猪-猴”异种器官移植临床前研究,以及8例“猪-脑死亡受试者”异种器官移植亚临床研究,应用到研究中的供体猪也从4基因、5基因编辑猪,逐渐升级到了6基因编辑猪。
潘登科表示,本次移植入终末期肾病患者体内的“猪肾脏”,即来源于一头超洁净设施中培育的“6基因编辑供体猪”。这头供体猪敲除了3种会引起人体“超急性排斥和急性体液性排斥”的猪抗原,转入了2种“人补体调节蛋白”和1种“人凝血调节蛋白”。
在本次手术前,潘登科团队对供体猪进行了一系列的基因鉴定与病原微生物检测,以确保它符合异种器官移植手术的要求。而手术后,团队还保存了供体猪的原始样品,以便后续能进行病原微生物、病原体的溯源。
此外,对于供体猪培育的未来计划,潘登科提到,当下的“6基因编辑供体猪”在肾脏、心脏、肝脏等异种移植的研究中的表现已较为理想,但团队未来还将进一步针对不同的器官需求,培育更加“个性化”的供体猪,“不同的器官从本身的差异、免疫排斥反应等方面看都略有不同。采用‘个性化’的供体猪,能在临床试验中取得更好结果。”
“猪器官”离惠及更多病人还远吗?
我国约有1.3亿慢性肾病患者,其中终末期肾病患者数量庞大且呈逐年上升趋势。每年新增大量终末期肾病患者靠透析维持生命,肾移植是治愈终末期肾病的唯一有效方法。但器官短缺的现状,导致许多患者在漫长等待中病情恶化,甚至失去生命。
西京医院成功完成上述手术后,窦科峰院士公开表示:“此次突破性研究,为终末期肾病患者临床救治提供了新思路,进一步证实异种移植应用于临床的可能性和有效性,未来,随着相关研究的持续深入与技术的不断完善,异种移植有望成为解决器官短缺问题的重要手段,为更多患者带来生命转机。”
那么,我国的基因编辑猪器官预计会在未来何时为更多人所用,开展正式的临床试验?潘登科认为最早的时间或许为2026年,“今年2月,美国批准了猪肾人体移植临床试验,预计会在未来的5~6年进入临床应用,我们也差不多在这个时间。”
记者留意到,在美国食品药品监督管理局(FDA)批准了猪肾人体移植临床试验后,美国两家生物技术公司联合治疗(UnitedTherapeutics)和eGenesis将于今年启动相关研究项目。其中联合治疗公司表示,这项试验最初将有6人参加,纳入55-70岁的终末期肾病患者,患者将在大约6个月的时间里受到密切监测,并终生随访。