本文系统地介绍了路易斯酸及其在催化领域的应用路易斯酸是接受电子对的物质,路易斯碱。文中通过分子轨道(HOMO/LUMO)理论进一步阐释了酸碱作用的电子本质。
路易斯酸碱理论由G.N. Lewis提出:是能够接受一对电子的物质,而是能够提供一对电子的物质。在路易斯酸碱反应中,碱将一对孤对电子捐出,与酸形成共价配位键(称为或);产物称为路易斯加合物或配合物。
路易斯定义较广泛,既包含传统的布朗斯特酸碱(质子酸碱)概念,也覆盖过渡金属配合物中的配位作用。在配合物中,配体提供孤对电子(路易斯碱),金属离子接受孤对电子(路易斯酸),所形成的配合物也是路易斯加合物。
路易斯碱换言之,如果分子HOMO接近非键态且能量较高,就倾向于提供电子对,表现为路易斯碱性质。例如NH₃的HOMO为非键轨道,因此能有效地向亲电物质提供电子。
路易斯酸如BeH₂分子由于其未占轨道易接受电子对而表现出路易斯酸性。总之,路易斯酸碱可用“受电子对者”和“供电子对者”来定义,MO理论则进一步解释了它们如何通过轨道相互作用而结合。
路易斯酸碱的反应机制
配位与活化金属路易斯酸与配体孤对电子配位时,会,使配体孤对原子表现得更“电负”或更稳定,从而显著增强基团对反应的亲电性。例如,金属离子与羰基氧配位后,会降低羰基的LUMO能量,使羰基碳更易被亲核试剂攻击。
一般来说,极性机理下路易斯酸配位会削弱键的稳定性(如促进卤素离去),或直接降低亲电基团的轨道能级,增强其活性。这种行为类似于布朗斯特酸催化,但路易斯酸不提供质子,只通过电子作用完成活化。
丹麦等人指出,路易斯碱不仅仅是路易斯酸的“补充”,它们能同时增强所配位分子的亲电性和亲核性,因而具有多样的催化功能。
受阻路易斯酸碱对总的来说,路易斯酸碱通过配位与电子转移,实现了底物活化和反应速率的提高,同时也影响立体化学和区域选择性。
路易斯酸碱在催化中的应用
这些催化剂可以作用于多种亲核添加或交换反应:Friedel–Crafts烷基化或酰基化Aldol反应亲核加成Diels–Alderene反应路易斯酸催化不仅加速反应速率,还往往能改变产物的立体化学:通过双配位(如双位点金属配位两端官能团)近年来,设计型含手性配体的路易斯酸催化剂被广泛开发,用于不对称催化合成。例如,基于手性BINOL、Spirik配体与金属离子的复合物,已成功实现对映选择性的环加成、烷基化等反应。
受阻路易斯酸碱对(FLPs)是一种兼具酸碱功能的新兴催化体系。由于结构阻碍,酸碱中心不能中和结合,从而保留了对H₂或CO₂等小分子的活化能力。途径。
相关文献
Stephan 等人(Science 2006)首次展示了一个金属自由的膦—硼受阻酸碱对,其化合物(C₆H₂Me₃)₂PH(C₆F₄)BH(C₆F₅)₂在高温下失去H₂,在室温下可重新吸附H₂,实现了可逆的金属自由氢活化。这一发现奠定了受阻路易斯酸碱对(FLP)催化的基础。
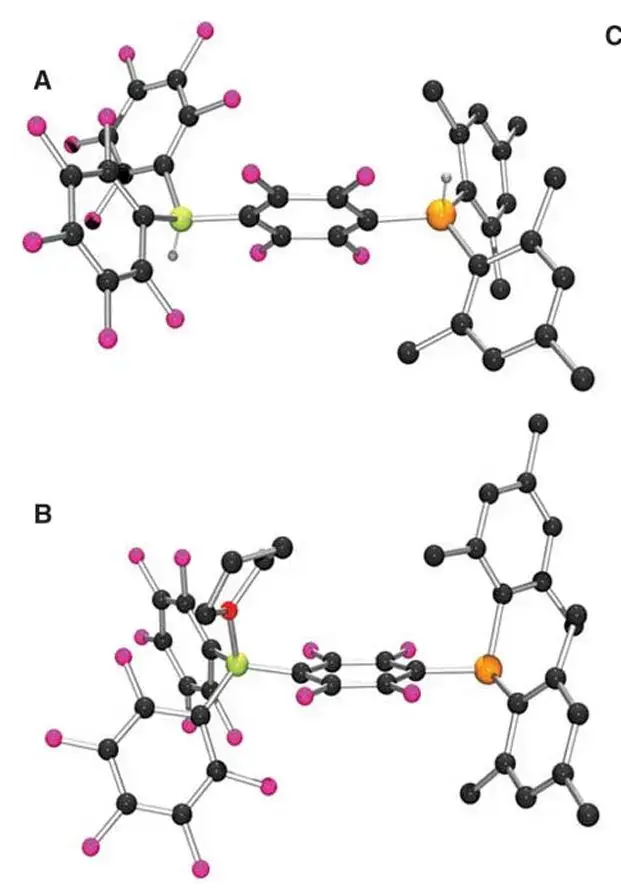
随后,Stephan 与 Erker(Angew. Chem. Int. Ed. 2010)对FLP体系进行了综述,指出体积庞大的碱和酸配对无法形成常规加合物,其未被“淬灭”的酸碱中心可协同裂解H₂并作为金属自由催化剂氢化取代基较大的亚胺、烯醚等。这类文献说明了路易斯酸碱在活化小分子和无金属催化氢化中的典型用法和优异性能。
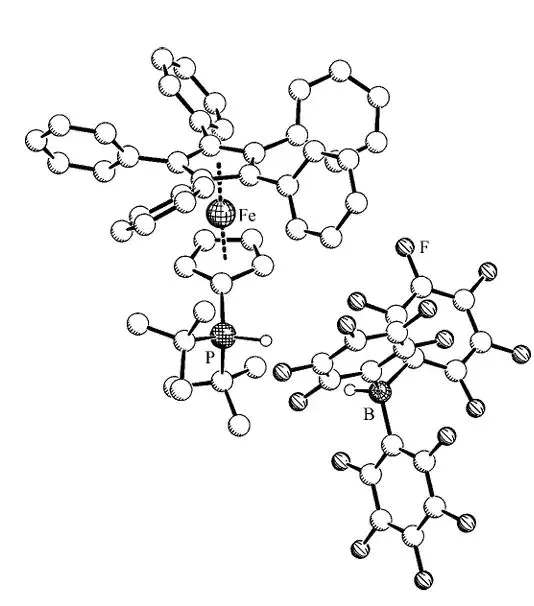
在有机合成催化中,Huang 等人(J. Am. Chem. Soc. 2017)报道了一种结合路易斯酸催化和光化学的创新策略:他们将底物与手性Rh(III)配合物形成配合物,利用可见光直接激发该配合物实现[2+2]光催化环加成。
10.1021/jacs.7b04363
他们将二茚醚基团引入4-氨基吡啶结构中,合成出高效的不对称酰基化催化剂。仅用0.5 mol%的催化剂,就能高效生成全碳季碳中心,产率接近定量,对映体过量达到98:2。