引言:靶向治疗的“双刃剑”
随着FDA最近推出的OPTI MUS项目推进,癌症治疗正从“一刀切”模式转向个性化医疗新时代。医生们开始问的不是“最大剂量是多少”,而是“最低有效剂量是多少”。未来五年,我们将看到更多基于血药浓度监测和基因检测的动态调整治疗方案,让肺癌患者在保持疗效的同时,真正实现高质量长期生存。
对于携带特定基因突变(如EGFR、ALK等)的非小细胞肺癌(NSCLC)患者而言,靶向治疗(Targeted Therapies, TT)的出现无疑是一场革命。这些精准打击癌细胞的药物显著改善了患者的生存状况,已成为各阶段治疗的标准方案[1,2]。然而,随着靶向药的广泛应用,新的问题也浮出水面:我们是否对患者进行了“过度治疗”?
目前,靶向药的剂量和疗程多是基于早期临床试验确定的,其核心逻辑源于传统化疗——剂量越大,疗效越好。但靶向药的作用机制与化疗截然不同,更高的剂量往往只带来更严重的毒副作用,而疗效却不一定成正比。此外,高昂的药费和长期的治疗给患者和全球医疗体系带来了沉重的经济负担,即所谓的“财务毒性”[3]。
因此,医学界开始探索一种新的治疗思路——治疗降级(De-escalation)。该策略旨在通过合理地降低药物剂量或缩短治疗时间,在不牺牲疗效的前提下,减轻患者的毒副反应、提升生活质量,并降低医疗成本。
一、为何能“减”?靶向治疗的独特逻辑
靶向药物如同一把“钥匙”,专门针对癌细胞上特定的“锁”(即驱动基因突变产生的异常蛋白),通过抑制其活性来阻断肿瘤生长。与化疗“杀敌一千,自损八百”的模式不同,靶向药的疗效更多取决于靶点结合亲和力、结合类型、靶点饱和度和避免耐药癌细胞中出现获得性激活通路的能力等因素,而非单纯的药物浓度[4]。
研究发现,许多靶向药达到有效抑制靶点所需的剂量,远低于其产生严重毒性(即最大耐受剂量,MTD)的剂量。然而,在药物研发早期,MTD常被选为推荐剂量(RP2D),这可能导致了系统性的“过量给药”[5]。一项对2020-2023年间新批准的31种靶向抗癌药的审查显示,其中20种都存在剂量优化的潜力[6]。为此,美国食品药品监督管理局(FDA)发起了“OPTIMUS计划”,旨在重新评估多种靶向药的最佳剂量,推动从“最大耐受剂量”向“最佳疗效和安全性剂量”的转变[7]。
二、剂量之辩:如何科学地“减量”?
降低剂量是治疗降级的核心策略之一。现有研究从多个角度探索了其可行性,并取得了一些积极成果。
01.降低每日固定剂量
多项研究表明,对于部分靶向药,较低的起始剂量或因副作用而减量,并未影响其长期疗效。
阿法替尼(Afatinib):一项回顾性研究显示,对于EGFR突变的晚期NSCLC患者,使用20mg或30mg的低剂量阿法替尼,其疗效可能与标准的40mg相当,且更适合亚洲患者[8]。对LUX-Lung 3和6试验的事后分析也证实,早期因不良反应而减量的患者,其无进展生存期(PFS)与未减量者无显著差异[9]。
阿来替尼(Alectinib):J-ALEX研究显示,300mg每日两次的剂量在日本ALK阳性患者中已表现出优异疗效,其PFS数据与全球ALEX研究中采用600mg每日两次的亚洲亚组数据相似[10,11]。这提示在不同人群中,更低的剂量或许同样有效,并能节约50%的成本。
索托拉西布(Sotorasib):在针对KRAS G12C突变NSCLC的Codebreak-100试验中,240mg/天的低剂量组与960mg/天的标准剂量组相比,PFS相似(5.4 vs 5.6个月),但客观缓解率(ORR)数值上略低(25% vs 33%)[12]。这说明并非所有药物减量都无损疗效,需要更多研究来界定。
注:新增氟泽雷塞、格索雷塞(KRAS G12C抑制剂)为后线I级推荐,删除索托拉西布(可能因疗效或安全性问题)。
02.改变服药频率
对于半衰期较长的药物,调整服药间隔是另一种创新的减量方式。
奥希替尼Osimertinib:该药半衰期长达48小时左右[13],理论上支持隔日服药(EOD)。一项小规模真实世界研究发现,对于经治患者,80mg隔日服药的中位总生存期(OS)可达14个月,优于40mg每日或隔日服药的方案[14]。目前,一项名为NCT05037331的II期临床试验正在前瞻性地评估这一方案的有效性和安全性。
03.“药效增强”新思路
“药效增强”(Boosting)策略是指联合使用一种药物(如CYP3A4抑制剂)来减缓靶向药在体内的代谢,从而在降低靶向药用量的同时,维持其有效的血药浓度。OSIBOOST试验初步证实了使用考比司他(cobicistat)增强奥希替尼药效的可行性[15]。这种方法为降低药费和毒性提供了新途径,但需警惕潜在的药物相互作用风险。
三、时间之问:何时可以“停药”?
除了减量,探索最佳治疗时长乃至适时“停药”,是降级策略的另一重要方向,尤其是在早期辅助治疗和晚期寡转移状态下。
01.辅助治疗:需要终身服药吗
在术后辅助治疗中,最佳疗程尚无定论。例如,ADAURA研究中奥希替尼辅助治疗为3年[1],而ALINA研究中阿来替尼则为2年[2]。长期服药不仅带来经济压力,患者的依从性也是巨大挑战。一项英国的真实世界分析显示,近四成患者会中断辅助奥希替尼治疗[16]。
未来,基于微小残留病灶(MRD)的动态监测,有望实现个体化的“适应性”辅助治疗。通过检测血液中的循环肿瘤DNA(ctDNA),可以判断术后体内是否还有残余的癌细胞。一项研究显示,在MRD检测不到的患者中暂停辅助奥希替尼治疗,仅有22.7%的患者在停药期间复发,提示MRD阴性或许是安全的“停药窗口”[17]。
02.晚期治疗:“药物假期”是否可行?
对于经过一线靶向治疗和局部巩固治疗(如放疗)后达到影像学完全缓解的寡转移患者,是否可以暂停系统治疗?一项前瞻性研究给出了积极信号[18]。该研究纳入了60名寡转移NSCLC患者,在达到完全缓解后暂停TKI治疗,并通过ctDNA进行监测。
患者的中位总停药时间达到9.1个月。
当监测到ctDNA转阳或疾病进展时,重新开始TKI治疗,缓解率高达96%。
这表明,在ctDNA指导下的“停药-再治”策略(即“药物假期”)是可行的,它不会影响再次治疗的敏感性,并能让患者在一段时间内免受药物副作用和经济负担的困扰。
四、现有证据与未来展望
目前,关于靶向治疗降级策略的研究正在全球范围内展开。下表总结了部分已完成和正在进行的重点临床试验。
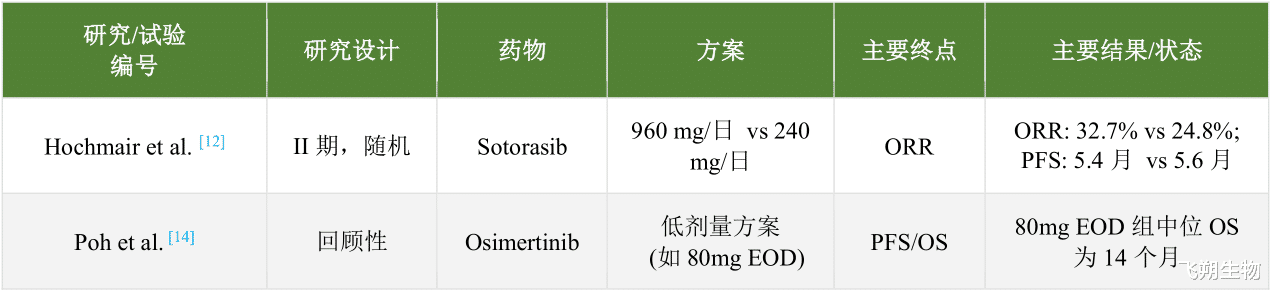
表1·非小细胞肺癌中部分靶向治疗降级策略的临床试验汇总
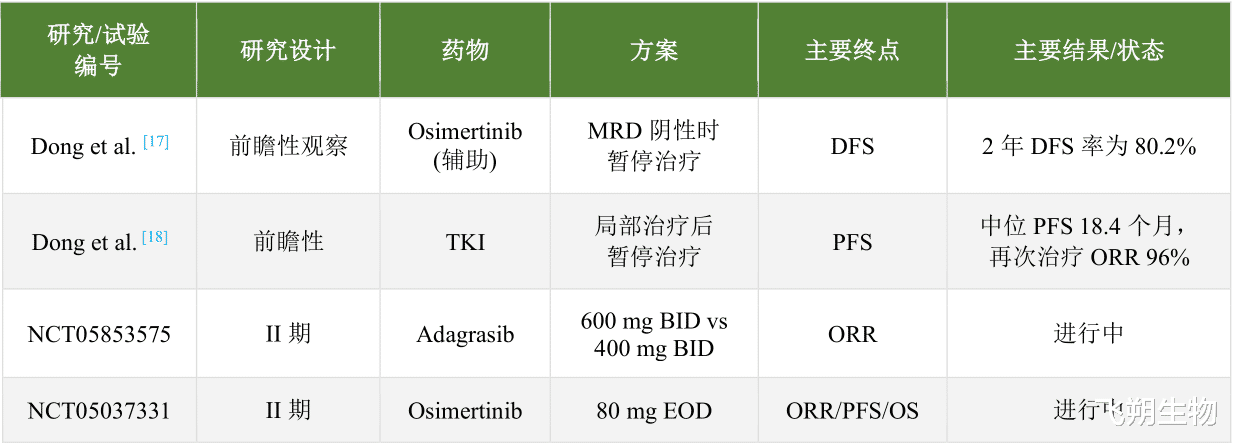
表2·非小细胞肺癌中部分靶向治疗降级策略的临床试验汇总
注:ORR: 客观缓解率; PFS: 无进展生存期; OS: 总生存期; DFS: 无病生存期; EOD: 隔日一次; BID: 每日两次; MRD: 微小残留病灶; TKI: 酪氨酸激酶抑制剂。
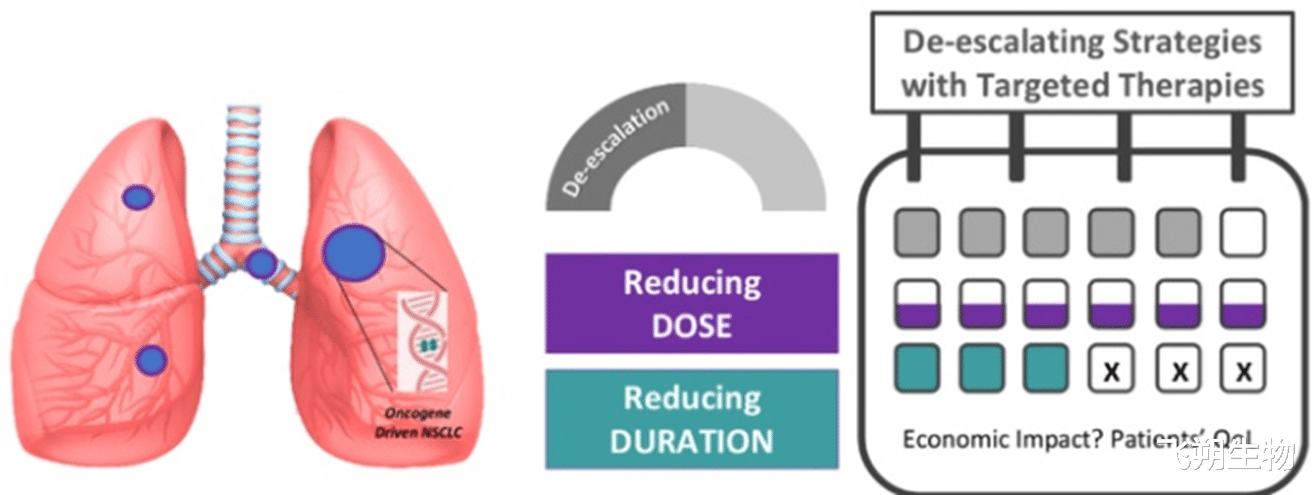
图1. 靶向治疗降级策略旨在通过减少剂量或缩短疗程,改善经济影响和患者生活质量(QoL)
尽管前景光明,降级策略的推广仍面临诸多挑战:
心理障碍:患者和医生都可能担心“减量/停药”等同于次优治疗,从而影响疾病控制。
耐药风险:间断治疗是否会加速耐药机制的出现,仍需长期数据验证。
标准缺失:目前缺乏标准化的筛选标准来确定哪些患者适合降级治疗,也缺少成熟的生物标志物来指导决策。
未来,需要更多设计严谨的非劣效性临床试验,并纳入生活质量、成本效益和患者报告结局(PROs)等综合性终点,为降级策略提供更高级别的证据。
结论
靶向治疗的“减法”哲学,代表了从“最大化治疗”到“最优化治疗”的理念转变。现有数据表明,在非小细胞肺癌领域,降低剂量或缩短疗程的降级策略是可行且有潜力的。这不仅有望减轻患者的身体和经济双重负担,更能推动全球癌症治疗走向更高效、更公平和更可持续的未来。当然,这一目标的实现,需要科研、临床、监管机构以及患者群体的共同努力和智慧。
参考文献
[1] N Engl J Med 2020; 383(18):1711–23.
[2] N Engl J Med apr. 2024; 390(14):1265–76.
[3] J Clin Oncol giu. 2023; 41(16): 3051–8.
[4] Cancers mar. 2020; 12(3):731.
[5] Lancet Oncol ago. 2024; 25(8):e340–51.
[6] N Engl J Med ott. 2021; 385(16):1445–7.
[7] Lung Cancer gen. 2020; 139:195–9.
[8] J Thorac Oncol lug. 2019; 14(7):1233–43.
[9] O.of the Commissioner, Project Optimus, FDA, giu. 2024.
[10] Transl. Lung Cancer Res. feb. 2024; 13(2):307–20.
[11] J. Eur. Soc. Med. Oncol. nov. 2016; 27(11):2103–10.
[12] Eur J Cancer set. 2024; 208:114204.
[13] Lung Cancer set. 2022; 171:97–102.
[14] Clin Pharmacol Drug Dev feb. 2019; 8(2):198–207.
[15] Lung Cancer Res. lug. 2024; 13(7).
[16] Ann Oncol set. 2024; 35: S782–3.
[17] JTO Clin. Res. Rep. nov. 2024.
[18] JAMA Oncol lug. 2024; 10(7):932.
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!
评论列表