免疫系统为什么打不过肿瘤?这个问题困扰了医学界很多年。
免疫检查点抑制剂这类药物已经让不少晚期患者受益,但仍有超过一半的人用药后效果不佳。原因是什么?《Science》杂志2026年4月的一项研究给出了一个出人意料的答案:问题出在免疫细胞的“电池”上。
这支研究团队发现,肿瘤微环境里的1型常规树突状细胞(cDC1s)——那些负责激活T细胞、启动抗肿瘤免疫反应的“指挥官”——它们的线粒体正在被肿瘤慢慢“耗死”。
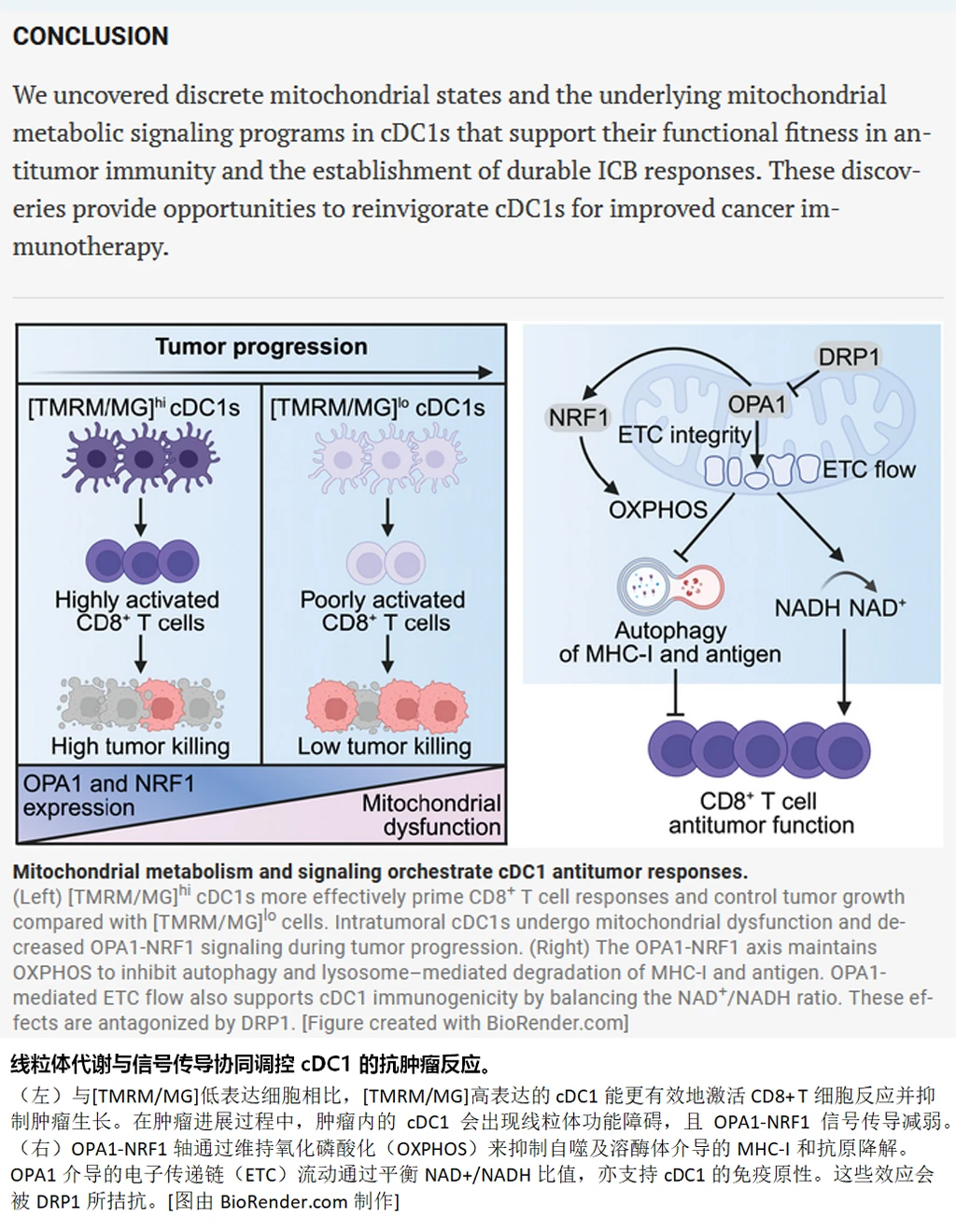
线粒体是细胞里的能量工厂。一个健康的cDC1,线粒体膜电位高、形态完整,能高效产出能量和信号分子,有力地向T细胞呈递肿瘤抗原。这样的细胞被标记为[TMRM/MG]高亚群。而功能失常的cDC1,线粒体去极化、碎片化,能量枯竭,连自己吞噬的抗原都保不住,直接被溶酶体降解了。这类细胞被标记为[TMRM/MG]低亚群。
肿瘤的狡猾之处在于,它不会一下子杀死这些免疫细胞,而是让它们的功能一点点衰退。随着肿瘤从早期进展到晚期,cDC1里的关键蛋白OPA1表达量下降了一半以上,线粒体体积萎缩,膜电位丢失。小鼠如此,人类肾癌和非小细胞肺癌患者的数据也一样。
OPA1是线粒体融合蛋白,负责维持线粒体网络的完整性。当OPA1减少,线粒体被分裂蛋白DRP1过度切割,变成一堆小碎片。这触发了两个致命后果:一是能量分子ATP骤降,二是NAD+/NADH比例失衡。能量危机激活了自噬,细胞开始“吃掉”自己的MHC-I分子和抗原——恰恰是激活T细胞最需要的东西。
研究人员做了一个大胆的尝试:从健康小鼠体内取出[TMRM/MG]高的cDC1,回输到荷瘤小鼠体内,再联合PD-L1抗体。结果是100%的小鼠肿瘤完全消退,而且60天后再次接种肿瘤细胞,小鼠依然有抵抗力——免疫记忆形成了。
这项研究的意义在于,它把癌症免疫治疗的思路从“解除T细胞的刹车”向前推了一步:在T细胞之前,树突状细胞的线粒体健康状态决定了整个免疫反应的起点。维持OPA1-NRF1轴的正常功能,保护线粒体的能量代谢和氧化还原平衡,可能成为下一代免疫治疗的新靶点。肿瘤在消耗免疫细胞的能量,而科学正在学习如何给免疫系统充电。