转自:药明康德
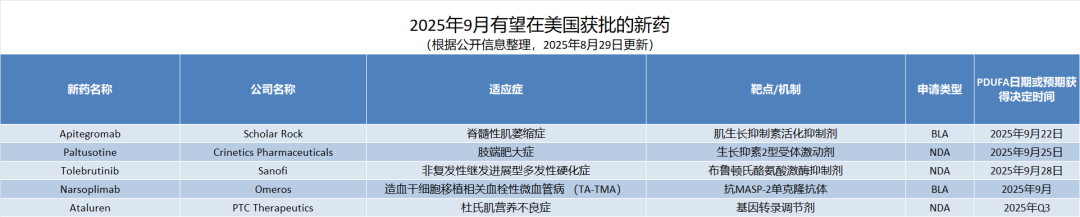
编者按:过去的2024年,美国FDA批准了超过60款创新疗法和疫苗。作为创新赋能者、客户信赖的合作伙伴以及全球医药及生命科学行业的贡献者,药明康德将持续通过独特的“CRDMO”业务模式,助力更多合作伙伴,为全球病患带来突破性创新疗法。根据PDUFA的目标日期,预计2025年9月,美国FDA将对5款创新药物的批准做出监管决定,本文将对这些疗法进行相关介绍。
活性成分:Apitegromab
适应症:脊髓性肌萎缩症(SMA)
公司名称:ScholarRock

Apitegromab是一种在研全人源单克隆抗体,通过选择性结合骨骼肌中肌生成抑制蛋白(myostatin)的前体及潜在形式,抑制其激活。根据新闻稿,它是首个在3期关键性临床试验中取得临床成功的SMA肌肉靶向候选药物。肌生成抑制蛋白属于TGFβ超家族成员,主要由骨骼肌细胞表达,其基因缺失与包括人类在内的多种动物种类肌肉质量与力量增加相关。美国FDA已授予该药物快速通道资格和孤儿药资格,以及罕见儿科疾病认定;欧洲药品管理局(EMA)也授予该药物PRIME资格和孤儿药资格,用于SMA治疗。
今年3月,ScholarRock宣布美国FDA已受理其为apitegromab递交的生物制品许可申请(BLA),用于治疗SMA患者。FDA同时授予这一申请优先审评资格,预计在今年9月22日之前完成审评。新闻稿表示,若apitegromab获批,将成为首款治疗SMA的肌肉靶向疗法。该公司同时宣布,EMA也已经接受apitegromab的上市许可申请(MAA)。
Apitegromab的监管提交资料基于关键性3期SAPPHIRE试验的积极疗效与安全性数据,同时还有2期TOPAZ试验及长期扩展ONYX试验的支持性数据。分析显示,SAPPHIRE试验达成了主要终点:与仅接受SMN靶向治疗(nusinersen或risdiplam)与安慰剂的患者相比,接受apitegromab联合SMN靶向治疗的SMA患者在汉默史密斯功能运动量表扩展版(HFMSE)评分中表现出统计学显著且临床意义明确的运动功能改善。
活性成分:Paltusotine
适应症:肢端肥大症
公司名称:CrineticsPharmaceuticals

Paltusotine(原名CRN00808)是一种口服非肽类生长抑素2型受体(SST2)选择性激动剂。该药设计为每日口服一次,用于控制肢端肥大症和类癌综合征相关症状。2024年12月,美国FDA接受了paltusotine的新药申请(NDA),拟用于成人肢端肥大症的治疗及长期维持治疗。根据新闻稿,如果获得批准,paltusotine将成为首款适用于成人肢端肥大症患者的每日一次口服SST2非肽激动剂。
在3期PATHFNDR-2研究中,每日口服一次paltusotine可维持肢端肥大症患者的胰岛素样生长因子1(IGF-1)水平和症状控制——IGF-1是内分泌专家用于管理肢端肥大症患者的主要生物标志物。分析显示,接受paltusotine治疗患者24周后达到IGF-1水平≤正常值上限的比例(56%)显著高于安慰剂组(5%,p